- Orbital molecular
-
En química cuántica, los orbitales moleculares son los orbitales (funciones matemáticas) que describen el comportamiento ondulatorio que pueden tener los electrones en las moléculas. Estas funciones pueden usarse para calcular propiedades químicas y físicas tales como la probabilidad de encontrar un electrón en una región del espacio. El término orbital fue utilizado por primera vez en inglés por Robert S. Mulliken en 1925 como una traducción de la palabra alemana utilizada por Erwin Schrödinger,'Eigenfunktion'. Desde entonces se considera un sinónimo a la región del espacio generada con dicha función. Los orbitales moleculares se construyen habitualmente por combinación lineal de orbitales atómicos centrados en cada átomo de la molécula. Utilizando métodos de cálculo de la estructura electrónica, como por ejemplo, el método de Hartree-Fock se pueden obtener de forma cuantitativa.
Contenido
Configuración electrónica
Los orbitales moleculares se utilizan para especificar la configuración electrónica de las moléculas, que permite describir el estado electrónico del sistema molecular como un producto antisimetrizado de los espín-orbitales. Para ello se suelen representar los orbitales moleculares como una combinación lineal de orbitales atómicos (también denominado LCAO-MO). Una aplicación importante es utilizar orbitales moleculares aproximados como un modelo simple para describir el enlace en las moléculas.
La mayoría de los métodos de química cuántica empiezan con el cálculo de los orbitales moleculares del sistema. El orbital molecular describe el comportamiento de un electrón en el campo eléctrico generado por los núcleos y una distribución promediada del resto de los electrones. En el caso de dos electrones que ocupan el mismo orbital, el principio de exclusión de Pauli obliga a que tengan espines opuestos. Hay que destacar que existen métodos más elaborados que no utilizan la aproximación introducida al considerar la función de onda como un producto de orbitales, como son los métodos basados en el uso de funciones de onda de dos electrones (geminales).
Obtención cualitativa de orbitales moleculares
Con el fin de describir cualitativamente la estructura molecular se pueden obtener los orbitales moleculares aproximándolos como una combinación lineal de orbitales atómicos.
Algunas reglas sencillas que permiten obtener cualitativamente los orbitales moleculares son:
- El número de orbitales moleculares es igual al número de orbitales atómicos incluidos en la expansión líneal.
- Los orbitales atómicos se mezclan más (es decir, contribuyen más a los mismos orbitales moleculares) si tienen energías similares. Esto ocurre en el caso de moléculas diatómicas homonucleares como el O2. Sin embargo en el caso de que se unan diferentes núcleos la desigual carga (y por tanto la carga efectiva y la electronegatividad) hacen que el orbital molecular se deforme. De esta manera los dos orbitales 1s del hidrógeno se solapan al 50% contribuyendo por igual a la formación de los dos orbitales moleculares, mientras que en el enlace H-O el oxígeno tiene un coeficiente de participación mayor y el orbital molecular se parecerá más al orbital atómico del oxigeno (según la descripción matemática de la función de onda)
- Los orbitales atómicos sólo se mezclan si lo permiten las reglas de simetría: los orbitales que se transforman de acuerdo con diferentes representaciones irreducibles del grupo de simetría no se mezclan. Como consecuencia, las contribuciones más importantes provienen de los orbitales atómicos que más solapan (se enlacen).
La molécula de hidrógeno
Como ejemplo simple, es ilustrativa la molécula de dihidrógeno H2, con dos átomos etiquetados H' y H". Los orbitales atómicos más bajos en energía, 1s' y 1s", no se transforman de acuerdo con la simetría de la molécula. Sin embargo, las siguientes combinaciones líneales sí lo hacen:
1s' - 1s" Combinación antisimétrica: negada por reflexión, inalterada por las otras operaciones 1s' + 1s" Combinación simétrica: inalterada por todas las operaciones En general, la combinación simétrica (llamada orbital enlazante) está más baja en energía que los orbitales originales, y la combinación antisimétrica (llamada orbital antienlazante) está más alta. Como la molécula de dihidrógeno H2 tiene dos electrones, los dos pueden ser descritos por el orbital enlazante, de forma que el sistema tiene una energía más baja (por tanto, es más estable) que dos átomos de hidrógenos libres. Esto se conoce como enlace covalente.
La aproximación de orbitales moleculares como combinación lineal de orbitales atómicos (OM-CLOA) fue introducida en 1929 por Sir John Lennard-Jones. Su publicación mostró cómo derivar la estructura electrónica de las moléculas de diflúor y dioxígeno a partir de principios cuánticos. Este acercamiento cuantitativo a la teoría de orbitales moleculares representó el nacimiento de la química cuántica moderna.
Tipos de orbitales moleculares
Al enlazar dos átomos, los orbitales atómicos se fusionan para dar orbitales moleculares :
- Enlazantes: De menor energía que cualquiera de los orbitales atómicos a partir de los cuales se creó. Se encuentra en situación de atracción, es decir, en la región internuclear. Contribuyen al enlace de tal forma que los núcleos positivos vencen las fuerzas electrostáticas de repulsión gracias a la atracción que ejerce la nube electrónica de carga negativa que hay entre ellos hasta una distancia dada que se conoce como longitud de enlace.
- Antienlazantes: De mayor energía, y en consecuencia, en estado de repulsión.
Los tipos de orbitales moleculares son:
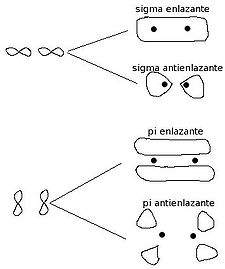
- Orbitales σ enlazantes: Combinación de orbitales atómicos s con p (s-s p-p s-p p-s). Enlaces "sencillos" con grado de deslocalización muy pequeño. Orbitales con geometría cilíndrica alrededor del eje de enlace.
- Orbitales π enlazantes: Combinación de orbitales atómicos p perpendicuales al eje de enlace. Electrones fuertemente deslocalizados que interaccionan fácilmente con el entorno. Se distribuyen como nubes electrónicas por encima y debajo del plano de enlace.
- Orbitales σ* antienlazantes: Versión excitada (de mayor energía) de los enlazantes.
- Orbitales π* antienlazantes: Orbitales π de alta energía.
- Orbitales n: Para moléculas con heteroátomos (como el N o el O, por ejemplo). Los electrones desapareados no participan en el enlace y ocupan este orbital.
Los orbitales moleculares se "llenan" de electrones al igual que lo hacen los orbitales atómicos:
- Por orden creciente del nivel de energía: Se llenan antes los orbitales enlazantes que los antienlazantes, siguiendo entre estos un orden creciente de energía. La molécula tenderá a rellenar los orbitales de tal modo que la situación energética sea favorable.
- Siguiendo el principio de exclusión de Pauli: Cuando se forman los orbitales atómicos estos podrán albergar como máximo dos electrones, teniendo estos espines distintos.
- Aplicando la regla de máxima multiplicidad de Hund: Los orbitales moleculares degenerados (con el mismo nivel de energía) tienden a repartir los electrones desapareándolos al máximos (espines paralelos). Esto sucede para conseguir orbitales semillenos que son más estables que una subcapa llena y otra vacía debido a las intensas fuerzas repulsivas entre los electrones. Gracias a ello podemos dar explicaciones a propiedades de ciertas moléculas como el paramagnetismo del oxígeno molecular (el orbital más externo de la molécula tiene electrones desapareados que interaccionan con un campo magnético)
Según estas reglas se van completando los orbitales. Una molécula será estable si sus electrones se encuentran de forma mayoritaria en orbitales enlazantes y será inestable si se encuentran en orbitales antienlazantes:
- Al combinar dos orbitales 1s del hidrógeno se obtienen dos orbitales moleculares sigma, uno enlazante (de menor energía) y otro
antienlazante (de mayor energía). Los dos electrones de valencia se colocan con espines antiparalelos en el orbital σ y el orbital σ*
queda vacío : la molécula es estable. - Al combinar dos orbitales 1s de helio se forman dos orbitales moleculares sigma y los cuatro electrones llenan todos los
orbitales. Sin embargo los orbitales antienlazantes fuerzan a la molécula a disociarse y se vuelve inestable, por ello no
existe molécula de He2.
Véase también
Wikimedia foundation. 2010.