- Elementos orbitales
-
Elementos orbitales
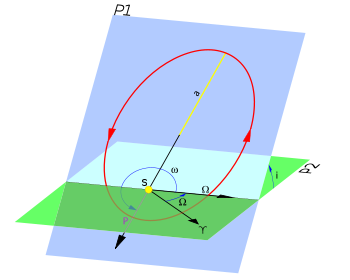 Elementos orbitales de un cuerpo alrededor del Sol
Elementos orbitales de un cuerpo alrededor del Sol
Los elementos orbitales de la órbita de un cuerpo celeste son un conjunto de seis cantidades que permiten definir su órbita alrededor del Sol o cualquier otro cuerpo celeste de forma totalmente unívoca. Estas seis cantidades son:
- Longitud del nodo ascendente (
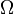 )
) - Inclinación de la órbita (
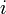 )
) - Argumento del perihelio (
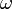 ). Si no es el Sol (Argumento del periastro)
). Si no es el Sol (Argumento del periastro) - Semieje mayor de la órbita (
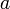 )
) - Excentricidad de la órbita (
 )
) - Anomalía media de la época (
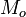 )
)
A veces, en lugar de la anomalía media de la época, se utiliza la anomalía media de un tiempo dado (
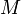 ), o la longitud media, o la anomalía verdadera o, raramente, la anomalía excéntrica.
), o la longitud media, o la anomalía verdadera o, raramente, la anomalía excéntrica.A veces la época del paso por el perihelio reemplaza a la anomalía media. En lugar del semieje mayor se puede utilizar también el período orbital.
A veces se usa la
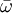 (longitud del periastro), que se relaciona con Longitud del nodo ascendente (
(longitud del periastro), que se relaciona con Longitud del nodo ascendente (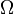 ) y el Argumento del periastro (
) y el Argumento del periastro (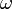 ) mediante:
) mediante:
Vemos que los primeros tres elementos orbitales simplemente son que los ángulos de Euler que definen la orientación de la órbita en el espacio. Mientras los tres siguientes definen la forma de la órbita y la posición del cuerpo en la órbita.- La inclinación y la longitud del nodo ascendente indican el plano de la órbita.
- El argumento de perihelio orienta la órbita dentro de su plano.
- El semieje mayor (o el período, indistintamente) determina el tamaño de la órbita.
- La excentricidad su forma.
- La época del paso por el perihelio (o la anomalía media) permiten situar al objeto en su órbita.
Los seis elementos anteriores surgen en el problema de los dos cuerpos sin perturbaciones externas. Una trayectoria perturbada realista se representa como una sucesión de cónicas instantánea que comparte uno de su focos. Estos elementos orbitales se llaman osculatrices y la trayectoria es siempre tangente a esta sucesión de cónicas.
Los elementos orbitales de objetos reales tienden a cambiar con el tiempo. La evolución de los elementos orbitales tiene lugar debido fundamentalmente a la fuerza gravitatoria de los otros cuerpos. En el caso de satélites, debido a la falta de esfericidad del primario, o al roce con los restos de atmósfera. Esto es fundamental en satélites artificiales de la Tierra o de otros planetas. En el caso de cometas la expulsión de gas, y la presión de la radiación, o las fuerzas electromagnéticas introducen pequeñas fuerzas no gravitatorias que hay que considerar para explicar su movimiento.Los elementos orbitales en dos líneas
Hay muchos programas de informática para el seguimiento de los satélites artificiales en órbita alrededor de la Tierra. Para que puedan funcionar se necesita alimentarlos con elementos orbitales recientes. Datos de más de 30 días dan resultados profundamente inexactos. Los elementos orbitales de los diferentes satélites se listan en código de texto y pueden estar en diferentes formatos. El más común es el NASA / NORAD, que dan los elementos orbitales de cada satélite empleando dos líneas [1], originalmente se diseñó para el uso con las antiguas tarjetas perforadas de 80 columnas, pero todavía están en uso porque es el formato más común.
Véase también
Enlaces externos
Categoría: Mecánica celeste - Longitud del nodo ascendente (
Wikimedia foundation. 2010.