- Dolichonyx oryzivorus
-
Tordo arrocero

Estado de conservación 
Preocupación menor (UICN 3.1)Clasificación científica Reino: Animalia Filo: Chordata Clase: Aves Orden: Passeriformes Familia: Icteridae Género: Dolichonyx
SwainsonEspecie: D. oryzivorus Nombre binomial Dolichonyx oryzivorus
(Linnaeus, 1758)[1]Distribución 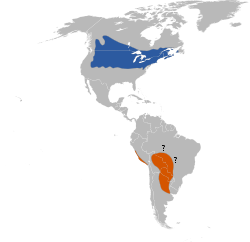
Azul: época de reproducción; Anaranjado: fuera de la época de reproducción.El tordo arrocero (Dolichonyx oryzivorus), también conocido como charlatán,[2] es un ave de hábitos migratorios perteneciente a la familia de los ictéridos, dentro del orden de los paseriformes, único miembro del género monotípico Dolichonyx. Vuela anualmente de las regiones templadas de América del Norte a Sudamérica centromeridional. Se trata de una especie gregaria[3] y poligínica, que se alimenta de granos y arroz, lo que llevó a que fuera considerada una plaga en algunas áreas; también consume insectos. Durante la época de reproducción, exhibe un marcado dimorfismo sexual que luego se disipa cuando el macho muda su plumaje por uno similar al de la hembra, poco antes de emprender su viaje al sur.[4] Es uno de los pocos paseriformes que experimentan dos mudas de plumas cada año.[2] Los tordos arroceros son aves de gran longevidad: viven comúnmente 5 o 6 años.[5] A pesar de que su número va en descenso, es considerada una especie bajo preocupación menor.[1] [2]
Contenido
Descripción
 Macho posado con su plumaje nupcial.
Macho posado con su plumaje nupcial.
Los tordos arroceros son más pequeños que la mayoría de los ictéridos.[6] En promedio, miden unos 18 cm de largo[7] —con longitudes de entre 15 y 21 cm—,[2] tienen una envergadura de alrededor de 29 cm[7] y un peso de unos 42 g[7] —con pesos de entre 29 y 56 g—.[2] El plumaje nupcial de los machos es predominantemente negro, con la nuca de color crema y la parte baja del dorso, la rabadilla y las plumas escapulares (aquellas que cubren la base del ala) blancos,[4] [8] siendo la única ave en Estados Unidos con el vientre negro y el lomo blanco y no al revés.[9] Fuera de la época de reproducción, se asemejan a las hembras, las cuales presentan una coloración mayormente beige, con vetas oscuras sobre el dorso, la rabadilla, los flancos y la cabeza.[10] La discreta coloración de las hembras las ayuda a camuflarse mientras anidan.[4] Los juveniles son similares a ellas pero más amarillentos y sin las vetas laterales.[2] [4] Cuando el macho acaba de mudar sus plumas en Sudamérica por su plumaje nupcial antes de emigrar al norte, sus nuevas plumas exhiben unas puntas amarillentas que luego desaparecen, dejando al descubierto la coloración negra y blanca.[2] La cola es corta, y el pico, corto, cónico, negro en los machos y pálido en las hembras.[2] Las plumas de la cola son puntiagudas.[4]
Distribución y migración
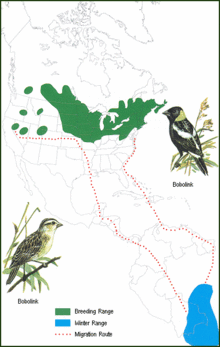 Verde: época de reproducción; azul: fuera de la época de reproducción; líneas punteadas: límites de la ruta migratoria típica.
Verde: época de reproducción; azul: fuera de la época de reproducción; líneas punteadas: límites de la ruta migratoria típica.
Sus áreas de reproducción incluyen campos abiertos de pasturas, especialmente campos de heno, en el norte de Estados Unidos y sur de Canadá.[3] [7] Anidan en esos lugares desde mayo hasta comienzos de julio.[10] Estas aves migran a las vastas llanuras y esteros[4] de Bolivia,[8] [11] el sudoeste de Brasil, Paraguay y el norte de Argentina para pasar allí los meses de primavera y verano australes entre noviembre y marzo.[10] [12] Es el único ictérido migrador neártico que llega hasta Argentina.[12] Poblaciones relativamente pequeñas pasan el invierno boreal en las costas de Perú y Chile.[10] Emprenden su regreso al norte a principios de marzo, alcanzando Colombia y Venezuela a finales de abril.[10] Desde allí, la mayoría continúa a través del mar Caribe hacia Florida, aunque algunos cruzan el golfo de México desde la península de Yucatán hacia Luisiana y Texas.[10] Seguidamente, se diseminan en dirección norte y oeste para llegar a sus áreas de reproducción en mayo.[10]
Después de una temporada reproductiva de nueve semanas, típicamente se congregan en pantanos para mudar su plumaje antes de dirigirse al sur a fines de agosto.[10] Se cree que los que anidan en el oeste de Estados Unidos y Canadá vuelan primero hacia la costa atlántica antes de rotar su curso hacia el sur. La migración procede a través de Florida y el Caribe, con paradas en Cuba y Jamaica.[10] Algunos ejemplares han sido avistados en las Bermudas en lo que pareciera ser un viaje sin escalas desde las regiones costeras comprendidas entre Virginia y Nueva Escocia a Sudamérica.[10] Tras alcanzar América del Sur en octubre, la mayoría pasa los siguientes dos meses intentando llegar a Bolivia,[8] [11] el sudoeste de Brasil, Paraguay y norte de Argentina.[10] La migración anual del tordo arrocero es una de las más largas del hemisferio occidental: hacen un viaje de aproximadamente 20.000 km.[2] [10]
Aunque los tordos arroceros viajan grandes distancias, rara vez han sido vistos en Europa; como sucede con muchas otras aves oriundas de América del Norte, la gran mayoría de estos avistamientos eventuales se produjo en las islas británicas.[8] [11]
Fluctuaciones históricas en su número y distribución
Las fluctuaciones históricas en la cantidad de ejemplares y su área de distribución reflejan los cambios en el paisaje y las prácticas agrícolas.[10] Los tordos arroceros anidaban originalmente en las praderas del medio oeste de Estados Unidos y Canadá centromeridional.[10] [13] Su área de distribución creció hacia el este y su número aumentó con la desforestación de los bosques nororientales, ampliando los campos de heno y praderas que utilizaban para anidar.[4] [10] [13] Originalmente las prácticas agrícolas favorecieron la expansión del área de distribución de la mayoría de las especies de aves de pastizales en el este de Estados Unidos porque mantenían la tierra libre de vegetación leñosa.[14] Para 1912, podía encontrársele a lo largo de todo el norte estadounidense y sur canadiense.[10]
Su apogeo se produjo probablemente hacia fines del siglo XIX cuando la agricultura se desarrolló y el uso generalizado del caballo como medio de transporte requirió grandes extensiones de heno.[10] [8] Los tordos arroceros se beneficiaban de la floreciente industria arrocera en el sudeste de Estados Unidos antes del comienzo del siglo XX, principalmente en los estados de Georgia y Carolina del Sur.[10] Enormes bandadas descendían sobre los arrozales para alimentarse antes de continuar su migración hacia Sudamérica.[10] Debido a que eran capaces de producir enormes daños a los cultivos, cientos de miles de ellos fueron masacrados y servidos en restaurantes.[10] En el Caribe, aún son cazados como alimento.[9]
Desde principios del siglo XX, su población se redujo, en especial en el este de Estados Unidos.[4] [14] [15] Su decrecimiento poblacional se debió mayormente a la masacre de bandadas migratorias en los arrozales del sur de dicho país,[4] la caza,[4] la modernización de las técnicas agrícolas,[4] el abandono de las granjas,[10] la disminución de las superficies cubiertas por heno,[10] [14] [15] las prácticas agrícolas cambiantes, la conversión de campos en bosques y el desarrollo de los terreno agrícolas durante las décadas de 1960 y 1970,[4] etc. Las técnicas agrícolas modernas —incluyendo rotaciones más frecuentes de los campos en los que se sembraba heno a otros cultivos,[4] [15] cosechas tempranas del heno[4] [14] [15] y el reemplazo de pastos de estación cálida a otros de estación fresca[4] — han vuelto los terrenos agrícolas menos favorables para la reproducción del tordo arrocero.[4] Asimismo, los campos de alfalfa (Medicago sativa), que ofrecen un hábitat reproductivo pobre a los tordos arroceros, han reemplazado muchos campos de Phleum pratense y fabáceas.[4] [10] [14] Las superficies cultivadas con heno en el noreste de Estados Unidos se redujeron de 12,6 a 7,1 millones de hectáreas desde 1940 a 1986, período en el cual los porcentajes de lugares en los que la alfalfa lo sustituyó se incrementaron de un 20% a un 60%.[4] La pérdida de su hábitat es en gran parte responsable por el decrecimiento de las poblaciones en Estados Unidos.[4] [8] Adicionalmente, el hecho de que en la actualidad los cultivos se cosechen más temprana y frecuentemente y el empleo de maquinaria moderna causan la muerte de muchas aves jóvenes.[2] [3] [10] Dentro del estado de Nueva Jersey, es considerada una especie amenazada desde 1979.[4] [9] La información de la North American Breeding Bird Survey, recopilada de observaciones de campo, señala un descenso de más del 90% en la población de tordos arroceros entre 1966 y 1992 en un área de 37.000 km² del norte de Illinois, el cual podría estar relacionado a una disminución en la superficie cubierta de pasturas, alfalfa y avenas en la zona.[16]
En el sudeste de Oregón, la colonización de la cuenca del lago Malheur por parte de los tordos arroceros se produjo recientemente en términos relativos puesto que no fueron detectados allí en estudios llevados a cabo en la década de 1870. Aparentemente, no hubo en la cuenca hábitats adecuados para la especie sino hasta 1872, cuando los rancheros comenzaron a drenar las tierras anegadas para convertirlas en pasturas. Los primeros especímenes fueron recogidos en 1908 y se registró su reproducción en el lugar por primera vez en 1918. Hacia la década de 1970, la población anidaba en el Malheur National Wildlife Refuge era la única que quedaba en el estado y, a pesar de estar confinada a un área de sólo 865 hectáreas y no exhibir una tendencia a expandir su distribución, constituía la población más grande al oeste de las Grandes Llanuras. También se han registrado poblaciones más pequeñas en otras partes de Oregón —ahora extintas—, noreste de California y otros estados y provincias canadienses occidentales. Sin embago, el origen de las poblaciones occidentales es discutido. La mayoría de los autores ha asumido que los tordos arroceros colonizaron el oeste recientemente con el advenimiento de la agricultura. Por otro lado, una segunda posibilidad sería que estas poblaciones constituyan los vestigios de una antigua distribución más amplia que datara de cuando la Gran Cuenca estaba cubierta por pastizales. Aunque la población del Malheur Refuge haya resultado de una colonización reciente, esa teoría podría aún ser válida debido a que los colonizadores podrían haber surgido de otras poblaciones occidentales. Sin embargo, la ausencia de subespecificación entre estas poblaciones sugiere que probablemente hayan resultado de una expansión reciente en la distribución, a no ser que el flujo genético entre las poblaciones occidentales y orientales haya permanecido en niveles elevados durante largos períodos de tiempo.[17]
En Sudamérica, a medida que más tierras fueron empleadas en el cultivo del arroz, los tordos arroceros se ganaron la reputación de plaga entre los agricultores, quienes han tomado medidas como dispararles para ahuyentarlos y el uso de agroquímicos.[2] [10] Asimismo, a veces son capturados y enjaulados para ser vendidos como mascotas.[10] [9] Irónicamente, son ahora considerados beneficiosos para la agricultura en Estados Unidos y Canadá, debido a que el grueso de su dieta durante la época de reproducción está constituido por insectos, muchos de los cuales son dañinos para los cultivos.[10] Además, la mayor parte de los alimentos vegetales que consumen durante esos meses son semillas de hierbas o de plantas sin valor comercial.[10]
Hábitat
Los tordos arroceros viven en hábitats agrícolas de baja intensidad productiva, como henares y pasturas, durante la temporada reproductiva. Asimismo, puede encontrárseles en campos exuberantes en barbecho y prados de pastos, herbáceas y flores silvestres. Los nidos son construidos a menudo en las áreas de mayor densidad y altura vegetativa. Aunque pequeños números pueden anidar en pastizales de entre 2 y 4 hectáreas, los campos de mayor extensión sustentan densidades más altas de parejas reproductivas. Utiliza hábitats similares a lo largo de su ciclo anual. Durante la migración, los tordos arroceros ocupan campos en barbecho y terrenos agrícolas, así como también pantanos costeros y de agua dulce. En Sudamérica, se les puede hallar en pastizales, pantanos, arrozales y granjas.[4]
En el este de Estados Unidos, los campos de heno constituyen un importante hábitat reproductivo para la especie. La abundancia de tordos arroceros en henares viejos —de ocho años o más— en un área estudiada en Nueva York era al menos un 67% mayor a la de cualquier otro tipo de hábitat en la zona y cuatro veces mayor que en las praderas del Medio Oeste. La cantidad de tordos arroceros aumentaba exponencialmente con el tamaño de los henares y era mayor en aquellos campos con menor superficie cubierta por alfalfa.[15]
Comportamiento
Se trata de una especie de hábitos principalmente granívoros —aunque también insectívoros—, diurnos en términos generales, gregarios, poligínicos, filopátricos y migratorios de larga distancia entre América del Norte y del Sur. El tordo arrocero migra durante la noche y aparentemente usa el campo magnético terrestre para orientarse.[10] De 215 especies neotropicales migratorias, Rodenhouse y otros (1992) listan al tordo arrocero entre las menos de diez que causan un daño significativo a los cultivos sobre amplias áreas geográficas.[18]
Los machos de tordo arrocero emiten dos tipos de canciones. No se ha encontrado evidencia de una función intersexual para una de ellas y una intrasexual para la otra. Los machos territoriales incrementan la cantidad de canciones de ambos tipos emitidas tanto en presencia de otros machos como de hembras. Sólo el 10% de las vocalizaciones emitidas por los machos son canciones de uno u otro tipo completas, mientras que el 87% son fragmentos de canciones y el restante 3%, canciones compuestas. Los machos territoriales reaccionan a la presencia de individuos de su mismo sexo aumentando la proporción de canciones fragmentadas y disminuyendo la de canciones compuestas. Incluyen menos notas por canción y emiten una mayor proporción de canciones que consistan sólo en las notas introductorias en presencia de estos. En conclusión, la respuesta vocal de los tordos arroceros machos territoriales a intrusos de su sexo consiste en cantar secuencias cortas y simples de cualquiera de los dos tipos de canciones.[19]
Alimentación
El tordo arrocero suele alimentarse en el suelo o posado en la vegetación.[2] [3] Su dieta está constituida por semillas, granos, insectos y arañas,[2] y puede representar un problema para los cultivos de arroz.[10] De hecho, el nombre científico de esta especie, oryzivorus, significa "comedor de arroz" en latín.[9] Mientras que los insectos representan la mayor parte de su dieta en su área de reproducción, éstos son reemplazados por los granos de cultivo mientras migra al sur.[3] [7] Si bien se alimenta típicamente durante el día, se le ha observado hacerlo en noches claras en arrozales cuando intenta almacenar reservas de grasa para su viaje a través del mar.[2]
Reproducción
En el sudeste de Oregón, las hembras escogen compañero entre aproximadamente el 20 de mayo y el 10 de junio y los nidos albergan polluelos desde alrededor del 11 de junio hasta el 7 de julio.[20] El macho corteja a la hembra en una postura también adoptada por otros ictéridos: la cabeza baja, las plumas del cuello infladas, la cola desplegada y las alas arqueadas hacia abajo, exhibiendo sus notorias manchas blancas en los hombros.[13] Esta especie cría a sólo una nidada por año.[21] [20] Ocasionalmente, es víctima del parasitismo de puesta por parte del tordo cabecicafé (Molothrus ater), un ictérido cuya reproducción requiere la puesta de sus huevos en los nidos de otras aves.[22] [23] En un estudio en henares en Nueva York en el que se siguió la evolución de 33 nidos de tordo arrocero, cada pareja produjo un promedio de tan sólo 0,3 polluelos que lograron abandonar el nido; mientras que el 85% de los nidos resultó improductivo debido a las prácticas agrícolas, otro 9% lo fue por causa de la depredación.[18]
Filopatría
Los tordos arroceros —especialmente los machos— demuestran cierta filopatría, es decir, tienden a regresar a las mismas áreas de reproducción año tras año.[5] Sin embargo, el éxito reproductivo en una determinada temporada influye en la elección del sitio de reproducción del año siguiente en ambos sexos.[24] Las hembras cuyas crías no hayan sobrevivido en un determinado lugar no son proclives a volver allí.[5] De manera similar, existe evidencia que indica que, entre los machos de cuyos nidos logra independizarse al menos un polluelo, aquellos que regresan a las mismas áreas a reproducirse en la temporada siguiente suelen haber tenido un éxito reproductivo significativamente mayor el año anterior que los que no lo hacen. En una investigación realizada en el estado de Nueva York entre 1982 y 1985, el 44% de los machos y el 25% de las hembras residentes en las áreas de estudio en una temporada volvieron en uno o más de los años siguientes. En los territorios de los machos que regresaban, se construían más nidos, se depositaban más huevos, eclosionaba un mayor número de estos y más polluelos lograban abandonar el nido que en los territorios de aquellos que no volvían en años siguientes. Asimismo, para las hembras filopátricas era mayor el número de huevos que eclosionaba y de polluelos que abandonaban el nido tanto en términos absolutos y como por huevo depositado, en comparación a las hembras que no regresaban.[24]
Nido y huevos
Los tordos arroceros anidan en colonias pequeñas y algo disgregadas.[6] La hembra remueve la vegetación para crear un espacio libre sobre el suelo en el que excava una pequeña depresión para el nido.[6] El nido, en forma de taza,[8] consiste en una pared externa de césped seco y tallos de hierbas con un recubrimiento interno de césped más fino y ciperáceas;[2] [10] las fibras son entretejidas con soltura.[6] Suele estar bien oculto en sitios en donde la hierba es densa y alta.[4] [8] La hembra deposita en él 5 o 6 huevos[7] [8] —ocasionalmente, entre 3 y 7 huevos—,[6] [10] de un color gris azulado o marrón rojizo pálido con manchas irregulares más oscuras, de 20,5 - 23,4 mm de largo por 15,1 - 17,3 mm de ancho.[2] El período de incubación varía entre los 11 y 13 días.[6] [2] Los polluelos son altriciales y adquieren la capacidad de volar entre 10 y 14 días después de haber eclosionado.[2]
Crianza de los polluelos
Ambos progenitores participan de la alimentación de la nidada.[8] En ocasiones, más de dos tordos arroceros alimentan a los jóvenes de un solo nido; puede encargarse de la tarea un adulto extra de cualquier sexo.[10] Existen diversas explicaciones para este comportamiento. Los análisis genéticos sugieren que en el caso de que el adulto extra sea un macho, tanto éste como el compañero de la hembra pudieron haber concebido a uno o más de los polluelos en el nido.[10] Puesto que esta especie muestra una marcada tendencia a regresar a las áreas en donde lograron criar a sus pequeños exitosamente o a donde ellos mismos fueron criados, los colaboradores pueden ser hijos de uno de los otros adultos o de ambos, nacidos el año anterior.[10] Otra posibilidad es que sean individuos sin ninguna relación de parentesco cuyos polluelos no hayan sobrevivido pero que aún conserven la necesidad biológica de alimentar a los jóvenes.[10]
El principal alimento dado a los polluelos son las larvas de lepidópteros y de avispas de sierra comunes (Tenthredinidae). En el sudeste de Oregón, estas representaban el 65,6% de la dieta de los polluelos en 1974, el 59,0% en 1975 y el 54,2% en 1976. En el mismo estudio, el intervalo promedio entre la eclosión de los polluelos primarios y la de los secundarios de los machos poligínicos fue de 6,0 días en 1973, 4,4 días en 1974, 3,8 días en 1975 y 7,2 días en 1976.[20]
En el sudeste Oregón, en donde los machos poligínicos usualmente alimentan a los polluelos secundarios, comienzan a hacerlo cuando los pequeños en el nido principal alcanzan determinada edad que varía de año en año. Asimismo, no es evidente ninguna relación entre la edad de los polluelos secundarios y el inicio de la colaboración del macho en su cuidado. Los machos continúan alimentando a los polluelos primarios después de comenzar a alimentar a los secundarios. La condición nutricional de los polluelos primarios es importante a la hora de determinar de qué manera los machos poligínicos distribuyen su esfuerzo en el cuidado de los pequeños. En los años en los que los polluelos primarios abandonan el nido con pesos elevados y no abren sus picos muy efusivamente al acercarse el investigador al nido —ambas, señales de un buen estado nutricional—, los machos poligínicos comienzan a alimentar a los polluelos secundarios pasados menos días desde su nacimiento.[20]
El comportamiento de los machos poligínicos justo antes de alimentar a los polluelos secundarios sugiere que aquellos podrían estar respondiendo directamente al estado de los polluelos primarios. Antes de aprovisionar a los nidos secundarios, los machos poligínicos casi invariablemente se posan primero cerca de sus nidos principales y dirigen sus cabezas hacia abajo, aparentemente para escuchar los agudos chillidos de sus polluelos. Sólo después suelen volar a los nidos secundarios y alimentar a sus pequeños allí, aunque otras veces se agachan y alimentan a los primarios. Ocasionalmente, los machos exhiben un comportamiento similar antes de ir en busca de alimento, posándose primero cerca de su nido principal y luego, del secundario, bajando su cabeza en cada oportunidad. Tras volver con alimento, generalmente repiten la secuencia antes de alimentar a los polluelos secundarios. En un caso extremo, un macho voló de su nido primario al secundario ida y vuelta cuatro veces, posándose y bajando su cabeza en cada ocasión, antes de finalmente alimentar a sus polluelos secundarios.[20]
Parasitismo de puesta y depredación en los nidos
A lo largo de su área de distribución reproductiva, rara vez el tordo cabecicafé (Molothrus ater) deposita sus huevos en nidos de tordo arrocero. En Ontario, 6 de 58 nidos registrados contenían huevos de tordo cabecicafé, lo que equivale a una incidencia parasítica de un 10,2% (Peck, 1975), mayor a la encontrada en cualquier otro sitio para esta especie.[23] En ocasiones, los tordos arroceros atacan a los tordos cabecicafé o emiten llamados de alarma en presencia de estos.[25] Los polluelos pueden sufrir la depredación de la grulla canadiense (Grus canadensis).[20]
Poliginia
Los machos son con frecuencia poligínicos,[8] con hasta cuatro hembras anidando simultáneamente en sus territorios.[10] Es probable que los machos poligínicos sean mayores y más experimentados y que, por lo tanto, puedan reclamar mejores territorios.[10] Estos dedican la mayor parte de su tiempo y atención a la primera compañera que hayan conseguido en la temporada y sus polluelos, asistiendo en la alimentación y la defensa de los pequeños en los nidos de otras compañeras sólo cuando el tiempo y los recursos lo permiten.[10] Según estudios llevados a cabo por Martin (1974) en Wisconsin, los machos poligínicos alimentan casi exclusivamente a los polluelos primarios —es decir, aquellos de su primera compañera— y sólo rara vez proporcionan alimento a los secundarios.[5] [20] Consecuentemente, la descendencia de las hembras secundarias está más expuesta a la desnutrición y puede experimentar una tasa de mortalidad más elevada.[5] [20] En el sudeste de Oregón, sin embargo, Wittenberger (1980) encontró que los machos poligínicos aprovisionaban regularmente tanto los nidos primarios como los secundarios.[20]
Los polluelos comienzan a pedir comida pocos minutos después de romper el cascarón. Durante los primeros días tras su eclosión, el macho y la hembra principal a menudo intercambian roles: mientras uno se queda dando calor a la nidada, el otro va en busca de alimento, pudiéndose alejar 400 o 500 m del nido. Esto les permite además seleccionar alimentos más grandes y nutritivos para traer de regreso. Así, los pequeños disponen de alimento y una temperatura adecuada de manera continua. En las mañanas frías, las hembras secundarias, en cambio, sólo pueden abandonar el nido por lapsos reducidos. Por esta razón, es probable que sus polluelos reciban menos alimento en un principio. En términos generales, sin embargo, la cantidad de comida conseguida por una hembra secundaria durante el proceso de crianza de sus hijos no es muy inferior a las cantidades conjuntas del macho y la hembra principal, estableciéndose cierto equilibrio.[5]
Adaptaciones de las hembras secundarias
Para adaptarse a estas desventajas, las hembras secundarias han desarrollado diversas estrategias. Por empezar, sus puestas son menos numerosas que la de la principal. El hecho de que la incubación comience antes de la puesta del último huevo asegura una eclosión asincrónica de los mismos; en tiempos de escasez de comida, el polluelo que haya eclosionado más tarde puede pasar hambre y ser aniquilado para evitar poner en riesgo la nidada entera. Asimismo, las hembras secundarias muestran una mayor tendencia a sacar provecho de los insectos que hallen en las cercanías del nido, dentro de los 60 m de éste, y son menos selectivas en cuanto al alimento. La asistencia parcial del macho en casos en los que las nidadas secundarias son excepcionalmente numerosas también es importante, contribuyendo a optimizar el desempeño reproductivo de estas aves.[5]
Nidadas reducidas
Una combinación de tres factores contribuye potencialmente a que las puestas de las hembras secundarias sean de menor tamaño. Uno de ellos es su edad fisiológica. Las que llegan primero a las áreas de reproducción —y, por ende, las que se convierten en las compañeras principales de los machos poligínicos— tienen al menos 2 años de edad. Un estudio siguió a 7 hembras nacidas el mismo año. En su primera aparición como ejemplares sexualmente maduros, éstas tardaron entre 1,5 y 2 semanas más que las aves de 2 años o mayores en alcanzar las áreas de reproducción y, en consecuencia, las 7 se convirtieron en compañeras secundarias de algún macho.[5]
Existe evidencia de que el número de huevos depositados aumenta con la edad. Esas mismas 7 hembras pusieron un promedio de 3,8 huevos en el primer año, 5,6 huevos en el segundo, 5,7 huevos en el tercero y 5,9 huevos en el cuarto. En conclusión, las hembras de mayor edad tienden a ser las compañeras principales de los machos y a tener nidadas más numerosas que las jóvenes, que adquieren un estatus secundario debido a su arribo tardío a las áreas de reproducción. Asimismo, es probable que una puesta reducida mitigue el estrés en hembras inexpertas en el cuidado de los polluelos.[5]
La renidificación es otro de los factores. Cuando el nido de una hembra es destruido, en ocasiones ésta permanece en la zona para construir uno nuevo. La segunda puesta siempre es uno o dos huevos más pequeña que la original. En estos casos, generalmente se emparejan con un macho en una relación secundaria. Cada año, después de las cosechas tempranas de la alfalfa, un cierto número de hembras con placas de incubación bien desarrolladas y vascularizadas —evidencia de una puesta reciente— aparece en los prados cercanos para volver a anidar.[5]
Por último, existe la posibilidad de una adaptación psicológica con respecto a su estatus. Aunque las compañeras de un mismo tordo arrocero macho no muestran un comportamiento de abierta animosidad entre ellas —como sí lo hacen las de tordo sargento (Agelaius phoeniceus) y tordo cabeciamarillo (Xanthocephalus xanthocephalus)—, las hembras principales a veces exhiben conductas agresivas hacia las secundarias, haciendo que éstas posiblemente tomen consciencia de su condición antes de la puesta de los huevos.[5]
Una hembra que ocupó el rol de compañera principal durante dos años depositó siete huevos en cada oportunidad. Al tercer año, también fue la hembra principal de un macho, pero su compañero desapareció en la fase de cópula, por lo que la hembra se apareó luego con otros machos; ese año su puesta consistió de sólo cinco huevos y no recibió ayuda en el cuidado de los polluelos. Al año siguiente, nuevamente como hembra principal, volvió a poner siete huevos. Otra hembra respondió de manera similar a este problema: su nidada como hembra principal de siete huevos un año se redujo a seis en la primavera siguiente tras la desaparición de su compañero; en su tercer año, depositó siete huevos otra vez. Ambos casos involucran puestas inusitadamente numerosas como hembras primarias. Probablemente, habrían afrontado dificultades si hubieran debido criar a siete polluelos sin la asistencia de un macho. Estos dos ejemplos sugieren que un estímulo derivado de ciertas relaciones intraespecíficas —o bien, de la falta de algunas interacciones— puede influir en la cantidad de huevos depositados.[5]
Eclosión asincrónica
Existe considerable evidencia de que la eclosión asincrónica o la matanza selectiva de parte de la nidada en favor del resto de la misma son comunes en algunas especies poligínicas, tales como el tordo tricolor (Agelaius tricolor), el chivirín pantanero (Cistothorus palustris), el tordo cabeciamarillo (Xanthocephalus xanthocephalus) y el tordo sargento (Agelaius phoeniceus). En el tordo arrocero, la incubación comienza tras la puesta del penúltimo huevo. Esto resulta en una eclosión asincrónica de los polluelos, en la que uno de ellos nace aproximadamente veinte o treinta horas después de sus hermanos. Si una hembra no pudiera mantener un suministro adecuado de alimentos, el más joven del nido rápidamente sufriría la falta de comida y sería aniquilado antes de que se desperdiciara alimento en un vano intento de salvar su vida. Esto incrementaría la inversión relativa de la hembra con respecto a la supervivencia de sus polluelos y aplacaría el riesgo de una intensa competencia entre los hermanos. Entre 1967 y 1972, este fenómeno representó la muerte de un promedio de 0,99 polluelos por nido secundario —entre 0 y 3, considerando los casos estudiados por separado— y de 0,26 polluelos por nido principal —de 0 a 2 en casos particulares—. Debido a las diferencias iniciales en el tamaño de las nidadas y las muertes resultantes de la eclosión asincrónica, los nidos secundarios contenían un promedio de 1,4 polluelos menos que los principales: 5,2 y 3,8 respectivamente. Esta característica de su biología reproductiva también se aplica a las hembras primarias bajo circunstancias desfavorables en las que la muerte de un polluelo garantiza la supervivencia de sus hermanos.[5]
En los años en los que hay una abundancia excepcional de alimento o condiciones climáticas benignas que permitan a las hembras secundarias embarcarse en expediciones más prolongadas en busca de alimento, todos los jóvenes tienen más posibilidades de estar debidamente nutridos. En estos casos, los polluelos más grandes se sacian, dando oportunidad a los más pequeños de obtener comida.[5]
La suma de puestas menos numerosas y la eclosión asincrónica aseguran a las hembras secundarias un éxito reproductivo variable, sensible a la disponibilidad de alimento. En condiciones apropiadas, la reducción de la nidada no es necesaria y las hembras sin ayuda de un macho son capaces de criar a todos sus polluelos. Cuando el alimento es insuficiente para cubrir satisfactoriamente las demandas de su descendencia, el último en romper el cascarón es rápida y eficientemente removido del nido. En este caso, sin embargo, las nidadas grandes requieren la eliminación de dos polluelos, uno de los cuales habrá eclosionado simultáneamente con la mayor parte de sus hermanos y consumiría una ración de comida que sería mejor invertida si se repartiera entre unos pocos sobrevivientes, pudiendo debilitar a todos ellos. Consecuentemente, si bien la reducción de la nidada puede ser un recurso importante para circunscribir la cantidad ya disminuida de polluelos en un nido, funciona óptimamente sólo cuando el tamaño de la puesta de una hembra secundaria se adecua con precisión a los suministros promedio de alimento de estos nidos.[5]
Flexibilidad en la atención por parte del macho
Como regla general, los machos no colaboran con sus compañeras secundarias en la crianza de los polluelos. No obstante, en casos en los que las puestas secundarias son inusualmente numerosas —5 o 6 huevos—, el macho divide su tiempo de manera desigual entre los jóvenes de la hembra primaria y los de las secundarias, concentrándose en los primeros, algunos días mayores. La asistencia de este en los nidos secundarios no suele darse sino hasta los 4 o 5 días de haber nacido los polluelos y es frecuentemente precedida de la reducción de la nidada. En esta instancia en la que las hembras se encuentran severamente sobreexigidas, la ayuda del macho indudablemente contribuye a la crianza de juveniles más sanos y fuertes y probablemente reduce el estrés de aquellas.[5]
Esto fue demostrado en un experimento en el que 6 polluelos de 3 días de edad fueron añadidos a 4 polluelos de 3 días en un nido secundario que hasta ese momento había sido ignorado por el macho, el cual se había estado ocupando de la alimentación de los 7 polluelos de 8 días de edad en el nido principal. Dentro de las dos horas de comenzado el experimento, el macho empezó a llevar comida al nido secundario, mientras aún dirigía la mayor parte de su atención a los hijos de la hembra principal. Dentro de los tres días, este nido secundario devino el centro de atención del macho. Tres de los polluelos murieron en el nido superpoblado, pero los otros 7 lograron abandonarlo gracias a la cooperación de ambos adultos. Esto quiere decir que los machos atienden a sus compañeras secundarias cuando estas tienen demasiado trabajo; pueden advertir las ocasiones en las que la crianza de una nidada excede la capacidad de un solo progenitor. En caso de depredación o pérdida del nido principal, los machos redirigen su esmero al nido secundario cuyos polluelos hayan eclosionado antes.[5] Sin embargo, a diferencia de sucedido entre los tordos cabeciamarillos (Xanthocephalus xanthocephalus) poligínicos en experimentos, es poco usual que un tordo arrocero macho redirija sus cuidados paternales a un nido secundario tras la reducción natural de su nidada primaria.[20]
Sobre el final de la temporada de reproducción, después de que los hijos de la hembra principal se hayan independizado, algunos machos comienzan a alimentar a los de la secundaria. Puede ser una adaptación por parte de las hembras secundarias el relegar la nidificación hasta un momento que minimice el período de superposición de dependencia de los polluelos primarios y los propios con respecto a sus padres. De este modo, los machos colaboran más frecuentemente con las hembras secundarias, cuyas nidadas pueden ser entonces de mayor tamaño. Este sorprendente comportamiento reproductivo ha sido identificado también en el chivirín pantanero (Cistothorus palustris); sin embargo, una posposición demasiado prolongada no es viable en los tordos arroceros debido a lo abreviado de su temporada de reproducción. En esta especie, pasan entre 45 y 50 días desde que los adultos encuentran pareja hasta que los polluelos se independizan de sus padres, y los jóvenes deben convertirse en fuertes voladores antes de su migración al sur.[5]
Resultado de las adaptaciones a la poliginia
El inferior tamaño de las nidadas secundarias, junto a la eclosión asincrónica, la gran regularidad con la que estas hembras alimentan a sus polluelos a pesar de no ser usualmente ayudadas por el macho y la plasticidad en los patrones de crianza por parte de éste evidenciada bajo circunstancias inusuales que requieren su asistencia en dichos nidos, constituyen una serie de importantes adaptaciones que impide un fracaso reproductivo masivo en las hembras secundarias. Esto, combinado con una flexibilidad en el sistema de emparejamiento que asegura que todas las hembras tengan la posibilidad de reproducirse en un hábitat donde las condiciones provean una oportunidad razonable de éxito, favorece la poliginia como estrategia reproductiva en ecosistemas en los que el alimento se encuentra generalmente concentrado.[5]
Referencias
- ↑ a b «Dolichonyx oryzivorus (Bobolink)» (en inglés). Lista Roja de la UICN. Unión Internacional para la Conservación de la Naturaleza (2011). Consultado el 11 de octubre de 2011.
- ↑ a b c d e f g h i j k l m n ñ o p q «Bobolink» (en inglés). All About Birds. Ithaca (Nueva York): Cornell Lab of Ornithology. Consultado el 29 de diciembre de 2010.
- ↑ a b c d e «Bobolink» (en inglés). South Dakota Birds and Birding. Consultado el 29 de diciembre de 2010.
- ↑ a b c d e f g h i j k l m n ñ o p q r s t u «New Jersey - Bobolink, Dolichonyx oryzivorus» (en inglés). Consultado el 29 de diciembre de 2010.
- ↑ a b c d e f g h i j k l m n ñ o p q r Martin, Stephen G. (1974). «Adaptations for Polygynous Breeding in the Bobolink, Dolichonyx oryzivorus» (en inglés). American Zoologist (Oxford University Press) 14 (1): pp. 109-119. http://icb.oxfordjournals.org/content/14/1/109.short. Consultado el 30 de diciembre de 2010.
- ↑ a b c d e f «Bobolink - Bird Web» (en inglés). Seattle Audubon Society. Consultado el 30 de diciembre de 2010.
- ↑ a b c d e f «Grassland Birds: Bobolink» (en inglés). The Nature Conservancy. Consultado el 29 de diciembre de 2010.
- ↑ a b c d e f g h i j k «Bobolinks, Dolichonyx oryzivorus: Information and Photos» (en inglés). Avian Web. Consultado el 30 de diciembre de 2010.
- ↑ a b c d e MacKenzie, Hall (2008). «The Endagered Species Spotlight - Bobolink» (en inglés). Tracks (Trenton (Nueva Jersey): Conserve Wildlife Foundation of New Jersey) 1 (2): pp. 1-2. http://www.conservewildlifenj.org/downloads/cwnj_6.pdf. Consultado el 4 de enero de 2011.
- ↑ a b c d e f g h i j k l m n ñ o p q r s t u v w x y z aa ab ac ad ae af ag ah ai aj ak al Deinlein, Mary (febrero de 1997). «Smithsonian Migratory Bird Center: Bobolink» (en inglés). Instituto Smithsoniano. Consultado el 28 de diciembre de 2010.
- ↑ a b c «Mystery Bird: Bobolink, Dolichonyx oryzivorus» (en inglés). Punctuated Equilibrium. The Guardian. Consultado el 29 de diciembre de 2010.
- ↑ a b Blanco, D. E.; López-Lanús, B., eds (2008) (en español). Introducción de “Ecología no reproductiva y conservación del Charlatán (Dolichonyx oryzivorus) en noreste de Argentina”. Buenos Aires (Argentina): Fundación Humedales / Wetlands International. ISBN 978-987-24710-0-2. http://lac.wetlands.org/Publicaciones/tabid/396/mod/1570/articleType/ArticleView/articleId/2245/Default.aspx. Consultado el 30 de diciembre de 2010.
- ↑ a b c «Bobolink Dolichonyx oryzivorus» (en inglés). eNature. Consultado el 30 de diciembre de 2010.
- ↑ a b c d e Bollinger, Eric K.; Blair Bollinger, Patricia; Gavin, Thomas A. (1990). «Effects of hay-cropping on eastern populations of the bobolink» (en inglés). Wildlife Society Bulletin (Allen Press) 18 (2): pp. 142-150. http://www.jstor.org/stable/3782128. Consultado el 12 de octubre de 2011.
- ↑ a b c d e Bollinger, E. K.; Gavin, T. A. (1992). «Eastern bobolink populations: Ecology and conservation in an agricultural landscape». En Hagan, J. M.; Johnston, D. W. (en inglés). Ecology and conservation of neotropical migrant landbirds. Washington D. C.: Smithsonian Institution Press. http://md1.csa.com/partners/viewrecord.php?requester=gs&collection=ENV&recid=2755781&q=Eastern+bobolink+populations%3A+ecology+and+conservation+in+an+agricultural+landscape&uid=790859755&setcookie=yes. Consultado el 11 de octubre de 2011.
- ↑ Herkert, James R. (abril de 1997). «Bobolink Dolichonyx oryzivorus population decline in agricultural landscapes in the Midwestern USA» (en inglés). Biological Conservation 80 (1): pp. 107-112. http://www.sciencedirect.com/science/article/pii/S0006320796000663. Consultado el 17 de noviembre de 2011.
- ↑ Wittenberger, James F. (1978). «The breeding biology of an isolated bobolink population in Oregon» (en inglés). The Condor (Cooper Ornithological Society) 80 (4): pp. 355-371. http://www.jstor.org/stable/1367186. Consultado el 20 de octubre de 2011.
- ↑ a b Rodenhouse, Nicholas L.; Best, Louis B.; O'Connor, Raymond J.; Bollinger, Eric K. (21-25 de septiembre de 1992). «Effects of temperate agriculture on neotropical migrant landbirds» (en inglés). General Technical Report RM-229 (Fort Collins (Colorado): Departamento de Agricultura de Estados Unidos, Servicio Forestal, Rocky Mountain Forest and Range Experiment Station): pp. 280-295. http://www.fs.fed.us/rm/pubs_rm/rm_gtr229/rm_gtr229_280_295.pdf. Consultado el 4 de abril de 2011.
- ↑ Capp, Michael S.; Searcy, William A. (1991). «An experimental study of song type function in the bobolink (Dolichonyx oryzivorus)» (en inglés). Behavioral Ecology and Sociobiology (Springer-Verlag) 28 (3): pp. 179-186. http://www.jstor.org/stable/4600533. Consultado el 9 de agosto de 2011.
- ↑ a b c d e f g h i j Wittenberger, James F. (1980). «Feeding of secondary nestlings by polygynous male bobolinks in Oregon» (en inglés). The Wilson Bulletin (Wilson Ornithological Society) 92 (3): pp. 330-349. http://elibrary.unm.edu/sora/Wilson/v092n03/p0330-p0340.pdf. Consultado el 10 de julio de 2011.
- ↑ «Bobolink Dolichonyx oryzivorus» (en inglés). Servicio Geológico de los Estados Unidos. Consultado el 31 de diciembre de 2010.
- ↑ «Brown-headed Cowbirds in Grasslands: Their Habitats, Hosts, and Response to Management» (en inglés). Departamento de Interior de los Estados Unidos, Servicio Geológico, Northern Prairie Wildlife Research Center (3 de agosto de 2006, fecha de última modificación cuando la página fue consultada). Consultado el 10 de febrero de 2011.
- ↑ a b Friedmann, Herbert; Kiff, Lloyd F.; Rothstein, Stephen I. (1977). «A further contribution to knowledge of the host relations of the parasitic cowbirds» (en inglés). Smithsonian Contributions to Zoology (Washington D.C.: Smithsonian Institution Press) 235: pp. 5-10. http://www.sil.si.edu/smithsoniancontributions/Zoology/pdf_hi/SCTZ-0235.pdf. Consultado el 26 de junio de 2011.
- ↑ a b Gavin, Thomas A.; Bollinger, Eric K. (febrero de 1988). «Reproductive correlates of breeding-site fidelity in bobolinks (Dolichonyx Oryzivorus)» (en inglés). Ecology (Ecological Society of America) 69 (1): pp. 96-103. http://www.jstor.org/stable/1943164. Consultado el 16 de noviembre de 2011.
- ↑ Robertson, Raleigh J.; Norman, Richard F. (1976). «Behavioral defenses to brood parasitism by potential hosts of the brown-headed cowbird» (en inglés). The Condor (Cooper Ornithological Society) 78 (2): pp. 166-173. http://elibrary.unm.edu/sora/Condor/files/issues/v078n02/p0166-p0173.pdf. Consultado el 8 de octubre de 2011.
Enlaces externos
 Wikimedia Commons alberga contenido multimedia sobre Dolichonyx oryzivorus. Commons
Wikimedia Commons alberga contenido multimedia sobre Dolichonyx oryzivorus. Commons Wikiespecies tiene un artículo sobre Dolichonyx oryzivorus. Wikispecies
Wikiespecies tiene un artículo sobre Dolichonyx oryzivorus. Wikispecies
Categorías:- Pájaros cantores (Passeriformes) no amenazados
- Icteridae
- Géneros de aves
- Aves migratorias del hemisferio occidental
- Aves de Argentina
- Aves de Bolivia
- Aves de Brasil
- Aves de Canadá
- Aves de Estados Unidos
- Aves de Paraguay
Wikimedia foundation. 2010.




